疫苗作為人類對抗疾病的核心手段之一,已從傳統的傳染病預防拓展至腫瘤、慢性感染和自身免疫性疾病等治療領域。預防性疫苗旨在激發健康個體對病原體的免疫防御,而治療性疫苗則致力于在患者體內重建或增強針對特定疾病靶點的治療性免疫應答。這兩類疫苗在目標人群、作用機制和預期臨床結局方向上的不同,使其在非臨床評價策略和要求上具有差異性。
本文將結合美國食品藥品監督管理局(FDA)、歐洲藥品監督管理局(EMA)、人用藥品技術要求國際協調理事會(ICH)及中國國家藥品監督管理局(NMPA)的相關指導原則,系統性分析預防性與治療性疫苗在非臨床試驗設計、核心評價內容及關注重點上的共性與特性,科學設計非臨床研究、規避研發風險、保障臨床受試者安全。
1
研究現狀
1.預防性疫苗
成熟領域:研發歷史悠久,技術平臺成熟(滅活、減毒、亞單位、多糖/結合、病毒樣顆粒、重組蛋白、病毒載體、mRNA/DNA 等)。
目標人群:主要針對目標人群為健康個體,以提前筑起應對傳染性疾病病原體(病毒、細菌、寄生蟲)的防線。廣泛覆蓋各年齡段,尤其重視嬰幼兒、老年人等脆弱人群。
評價體系:非臨床和臨床評價體系相對完善,全球接種覆蓋率持續提升,監管路徑較為清晰。關注點集中在健康人群的安全性(特別是局部/全身反應、過敏/自身免疫風險)和誘導強效、持久保護性免疫的能力。
2.治療性疫苗
新興領域:治療性疫苗作為免疫治療領域的重要分支,主要聚焦于腫瘤治療性疫苗(腫瘤新抗原疫苗、腫瘤相關抗原疫苗:如治療性HPV疫苗、個性化疫苗、基于樹突狀細胞的疫苗等)、慢性感染性疾病(治療性乙肝疫苗、治療性HIV疫苗等,旨在實現功能性治愈或長期控制)以及自身免疫性疾病與過敏(如針對自身抗原的耐受原性疫苗,以及針對過敏原的脫敏疫苗)。
目標人群:已患病的個體,常伴隨基礎疾病狀態、免疫系統異常(抑制或過度活化)及多種聯合用藥。
評價體系:非臨床評價面臨更高程度的復雜性。
機制復雜:需打破免疫耐受、增強或重塑已存在的(但無效或有害的)免疫反應;
模型瓶頸:建立能可靠模擬人類疾病病理生理及免疫微環境的動物模型是核心難點;
免疫應答復雜性:評估的免疫應答不僅需可被檢測,更需證明其具有明確的治療功能(如清除腫瘤細胞、抑制病毒復制、誘導免疫耐受);
安全性考量升級:需考慮疾病狀態本身、合并用藥對疫苗安全性和免疫原性的影響,以及長期免疫調節帶來的獨特風險(免疫抑制、過度激活、自身免疫等)。
2
相關指導原則
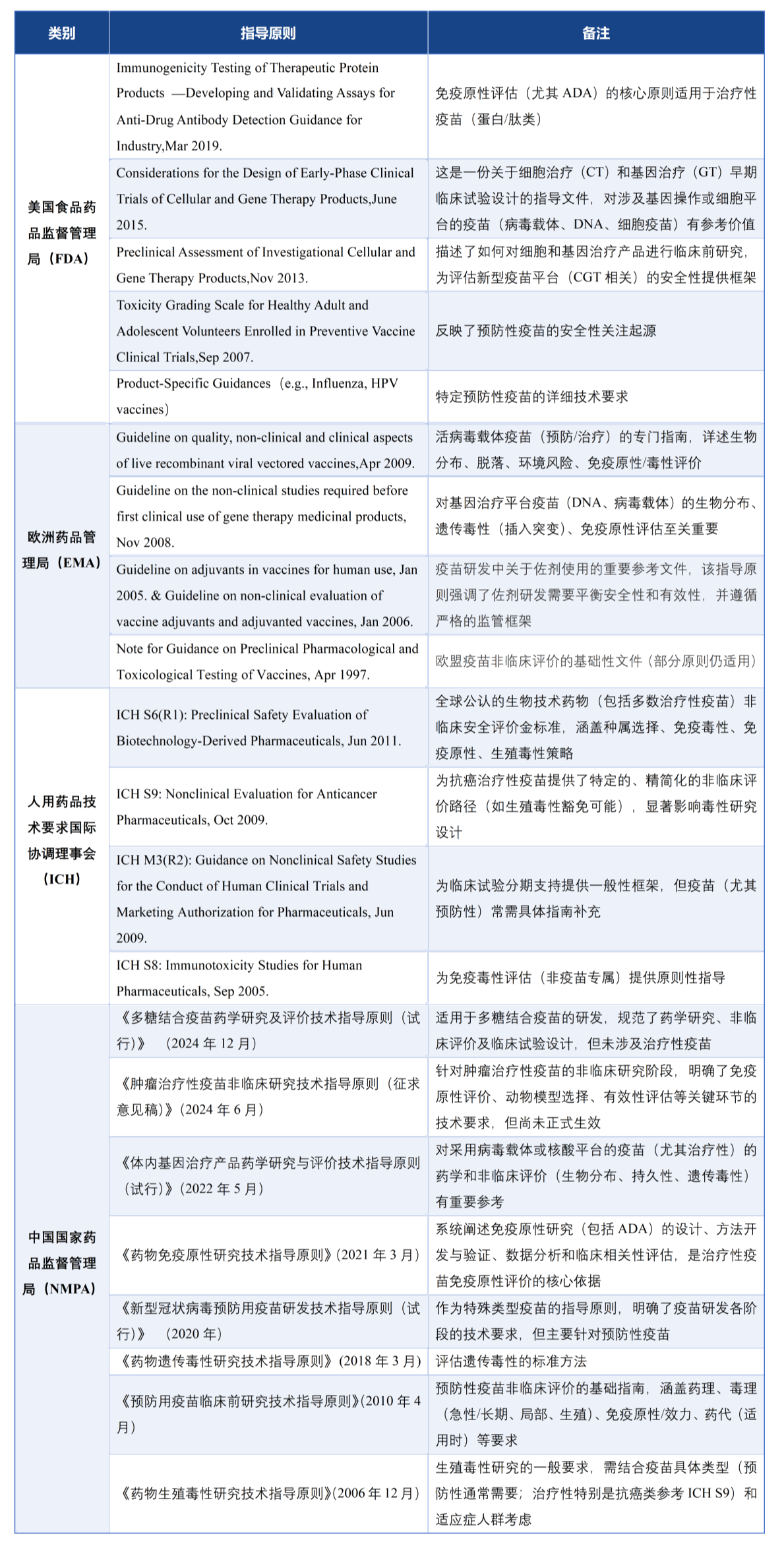
3
需要開展的非臨床安全性評價項目
——共性與差異分析
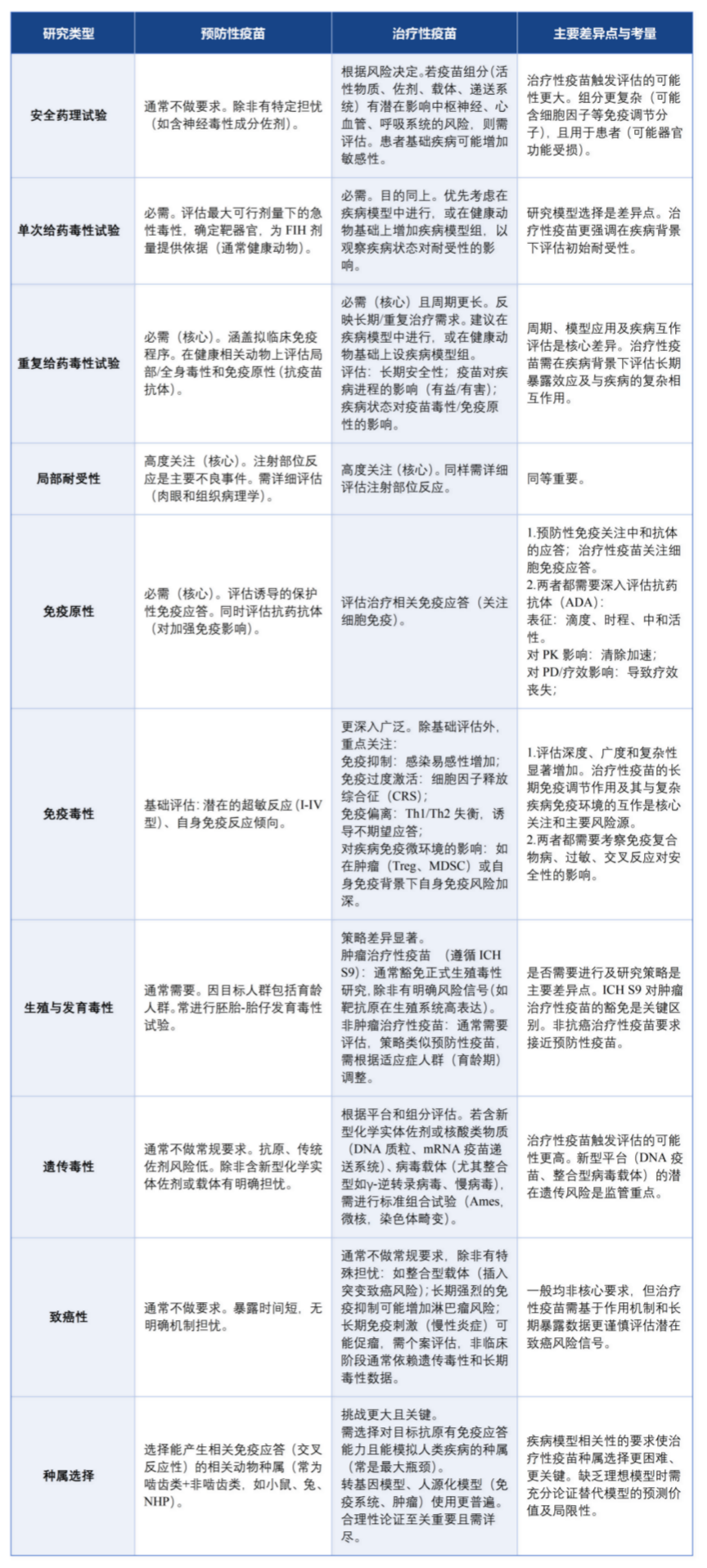
4
治療性疫苗試驗主要關注點
1.免疫原性與免疫毒性的深度評估(治療性疫苗核心):
精細區分:必須設計實驗區分治療性/保護性免疫應答與不良免疫反應(ADA、免疫偏離、自身免疫、超敏、CRS、免疫抑制)。
ADA核心地位:ADA的檢測、表征(中和能力)、對PK/PD/安全性的影響是治療性疫苗非臨床評價的重中之重。
免疫毒性譜系:全面評估免疫抑制/激活、自身免疫風險、免疫偏離、對疾病免疫環境的影響,需超越預防性疫苗的基礎要求。
2.動物模型與種屬合理性(治療性疫苗瓶頸):
疾病模型預測性:尋找/建立能可靠模擬人類疾病病理生理、免疫微環境和對疫苗治療反應的模型是首要挑戰,需明確模型局限性。
種屬相關性強論證:詳盡論證所選種屬在靶抗原表達/功能、免疫應答特性(受體、信號通路)、疾病發病機制上與人類的相似性。人源化模型需評估人源化程度和功能。
3.新型平臺技術(病毒載體、核酸疫苗、細胞疫苗)的特殊風險:
生物分布與持久性:明確載體/核酸/表達產物的組織分布(特別是生殖腺、中樞神經)、持續時間、清除動力學等。
載體/核酸免疫原性:抗載體免疫對初次及加強免疫的影響。
遺傳毒性/插入突變:DNA疫苗和整合型病毒載體的基因組整合潛能及后果評估是監管重點(需遺傳毒性試驗)。
局部/全身炎癥反應:如mRNA-LNP疫苗的反應原性(發熱、疲勞等),新型佐劑的炎癥潛能。
環境風險(活載體疫苗):評估脫落(排泄物、體液)、傳播給接觸者或環境的可能性及后果。
4.佐劑與遞送系統評價:
單獨與聯合評價:新型佐劑(如TLR激動劑、新型乳液、CpG)和遞送系統(LNP)需評估其自身毒性、免疫調節特性,以及與抗原組合后的效應(協同/拮抗)。
免疫毒性關注:強佐劑潛在的自身免疫誘導風險(需專門模型評估)、過度炎癥反應。
5.患者群體特殊性與聯合用藥(治療性疫苗):
基礎疾病影響:非臨床評價需考慮疾病狀態(如免疫抑制、肝腎功能損傷)對疫苗安全性、免疫原性和PK的潛在影響。在疾病模型中進行研究是關鍵。
計劃性聯合治療:若臨床計劃與其他療法(如免疫檢查點抑制劑、化療)聯用,非臨床階段應探索聯合給藥的潛在增效作用和安全性特征。
5
結語
預防性與治療性疫苗的非臨床評價,均以保障人體安全為核心目標,以基礎GLP和核心毒性研究(單次/重復劑量、局部耐受性)為框架。但兩者內在屬性和應用場景的差異(健康人群的預防性免疫激發vs患者群體的治療性免疫重塑),使其非臨床評價策略和要求有一定差別。
預防性疫苗:評價重點在于健康個體中良好的安全性特征(特別是局部/全身反應性、過敏/自身免疫風險的可控性)和誘導強效、持久保護性免疫應答的能力。相對成熟的模型體系和評價標準使其路徑較為清晰。
治療性疫苗:評價面臨顯著更高的科學和監管復雜性,核心在于:疾病模型中的驗證、免疫原性的深度剖析、復雜免疫毒性風險的識別、疾病背景下的長期安全性以及種屬與模型合理性的嚴格論證,這是支撐整個非臨床數據外推至人體的科學基礎。
在研究實踐中,需緊密結合具體疫苗的分子特性(抗原、佐劑)、技術平臺(傳統、病毒載體、核酸、細胞)、遞送系統及目標適應癥,制定出兼具科學性、靈活性且符合多區域監管要求的非臨床研究策略。這是保障疫苗研發安全、推動項目成功的關鍵所在。
為了應對疫苗療法對免疫評價的嚴苛要求,有濟醫藥配備了頂級的分析儀器與成熟的方法學開發能力,幫助疫苗產品成功從實驗室走向臨床。
高靈敏度免疫分析平臺
MSD:采用專利SULFO-TAG技術,顯著降低基質干擾,實現寬線性范圍和高靈敏度檢測,尤其適用于低豐度抗體的捕獲。
ELISA:建立自動化工作站,提升通量與重復性,滿足大批量樣本篩選。
功能性細胞免疫評估平臺
ELISpot:作為評估T細胞應答的“金標準”,能夠準確量化抗原特異性T細胞的頻率(IFN-γ、IL-2等)。
流式細胞術
多色 panel 設計能力:可定制9色以上流式方案,實現T細胞耗竭標志物(PD-1、TIM-3、LAG-3)、活化標志物(CD69、CD137、CD107a) 及胞內細胞因子的同步檢測。
免疫分型:精細區分T、B、NK、樹突狀細胞亞群,評估免疫調節劑或治療性疫苗對免疫系統的整體影響。
免疫毒性預警:通過Treg/Th17平衡、細胞因子風暴相關指標監測,早期識別潛在免疫毒性風險。
方法學開發與驗證能力
技術骨干擁有多年GLP實驗室經驗,擅長應對挑戰性樣本,確保方法的特異性、耐受性和可重復性。